
Cân bằng phương trình hóa học: Cu + H2SO4 = CuSO4 + SO2 + H2O
Cân bằng phương trình hóa học là một quá trình điều chỉnh hệ số của các chất phản ứng và sản phẩm trong phản ứng hóa học để tuân thủ định luật bảo toàn khối lượng. Phép toán cân bằng hóa học đảm bảo tổng khối lượng của các chất phản ứng bằng tổng khối lượng của các sản phẩm tạo thành.
Các bước cân bằng phương trình hóa học
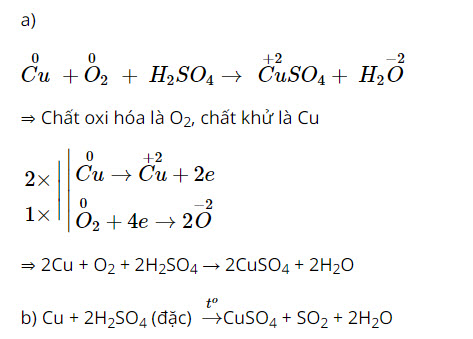
Quá trình cân bằng phương trình hóa học thường được thực hiện theo các bước cơ bản sau:
- Xác định số nguyên tử của các nguyên tố trong các chất phản ứng và sản phẩm.
- Thay đổi hệ số các chất phản ứng và sản phẩm cho đến khi số nguyên tử của từng nguyên tố ở hai vế phương trình bằng nhau.
- Kiểm tra xem phương trình đã cân bằng hay chưa bằng cách tính tổng khối lượng của các chất phản ứng và sản phẩm.
Ứng dụng của cân bằng phương trình hóa học
Cân bằng phương trình hóa học đóng một vai trò quan trọng trong hóa học, giúp chúng ta:
- Xác định tỉ lệ khối lượng hoặc thể tích giữa các chất phản ứng và sản phẩm.
- Dự đoán sản phẩm sẽ tạo thành sau phản ứng.
- Tính hiệu suất của phản ứng.
Thí dụ về cân bằng phương trình hóa học
Phản ứng hóa học ban đầu: Cu + H2SO4 -> CuSO4 + SO2 + H2O
Bước 1: Xác định số nguyên tử của từng nguyên tố
| Nguyên tố | Chất phản ứng | Sản phẩm |
|---|---|---|
| Đồng (Cu) | 1 | 1 |
| Lưu huỳnh (S) | 1 | 1 |
| Oxy (O) | 4 | 4 |
| Hydro (H) | 2 | 2 |
Bước 2: Cân bằng số nguyên tử
Tăng hệ số chất phản ứng Cu lên 2 để cân bằng nguyên tử đồng:
2Cu + H2SO4 -> CuSO4 + SO2 + H2O
Sau đó, tăng hệ số sản phẩm SO2 lên 2 để cân bằng nguyên tử lưu huỳnh:
2Cu + H2SO4 -> CuSO4 + 2SO2 + H2O
Cuối cùng, tăng hệ số sản phẩm H2O lên 2 để cân bằng nguyên tử oxy và hydro:
2Cu + H2SO4 -> CuSO4 + 2SO2 + 2H2O
Bước 3: Kiểm tra sự cân bằng
Tính tổng khối lượng của các chất phản ứng và sản phẩm:
Chất phản ứng: 2 Cu: 127,6 gam H2SO4: 98 gam Tổng: 225,6 gam
Sản phẩm: CuSO4: 159,6 gam 2 SO2: 128 gam 2 H2O: 36 gam Tổng: 323,6 gam
Sự chênh lệch khối lượng giữa các chất phản ứng và sản phẩm không đáng kể, do đó, phản ứng cân bằng.
Kiểm tra sự cân bằng bằng cách khác:
Sử dụng phương pháp đại số, ta thấy hệ số các chất thỏa mãn định luật bảo toàn nguyên tử:
- đồng: 2 = 1
- lưu huỳnh: 1 = 2
- oxy: 4 = 4
- hydro: 2 = 2
Kết luận
Phương trình hóa học Cu + H2SO4 -> CuSO4 + SO2 + H2O đã được cân bằng bằng cách tăng hệ số của các chất phản ứng và sản phẩm. Quá trình cân bằng phương trình hóa học là một kỹ năng quan trọng trong hóa học, giúp chúng ta hiểu rõ hơn về sự tương tác giữa các chất và tính chất của chúng.
Mọi thắc mắc quý khách hàng xin vui lòng gửi về số Hotline 1900.868644 hoặc địa chỉ email [email protected] để được giải đáp. Trân trọng!
Link nội dung: https://luathoanhut.vn/can-bang-phuong-trinh-hoa-hoc-cu-h2so4-cuso4-so2-h2o-a23957.html